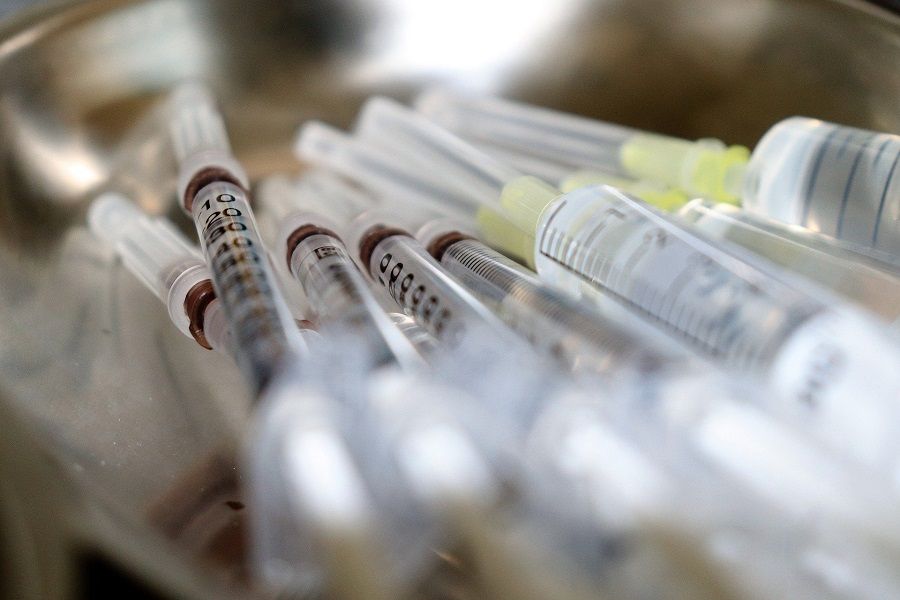
Trwają prace nad polską szczepionką przeciwko COVID-19 ?
Ten post dostępny jest także w języku:
![]() English
English

Ten post dostępny jest także w języku:
![]() English
English

Ten post dostępny jest także w języku: English Facebook Twitter LinkedIn Firma BioNTech ogłosiła utworzenie regionalnej siedziby w Azji Południowo-Wschodniej…

Ten post dostępny jest także w języku: English Facebook Twitter LinkedIn Ruszył zakład produkcyjny Medezin w inwestycji 7R Park Łódź…

Ten post dostępny jest także w języku: English Facebook Twitter LinkedIn Pandemia koronawirusa, choć groźna w swoich skutkach dla większości…
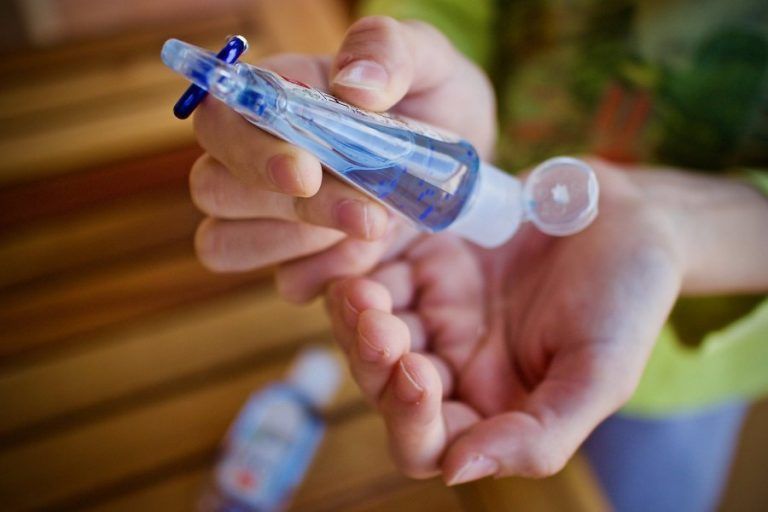
Ten post dostępny jest także w języku: English Facebook Twitter LinkedIn Jak wynika z danych opublikowanych przez Ministerstwo Zdrowia, w…
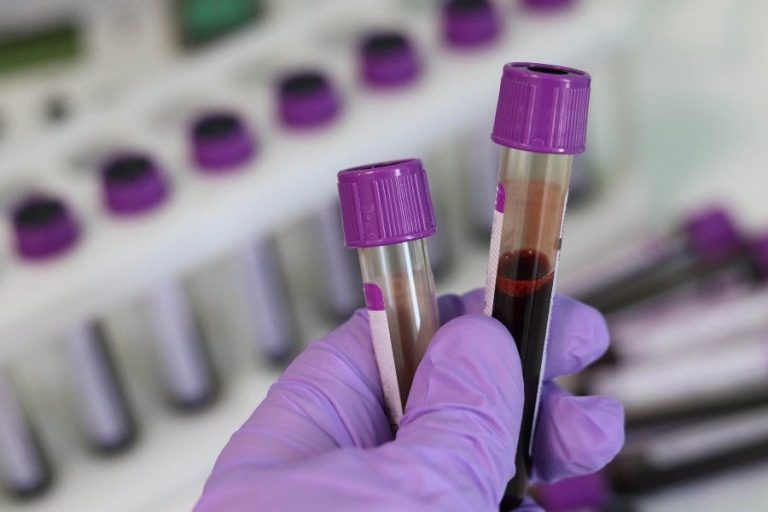
Ten post dostępny jest także w języku: English Facebook Twitter LinkedIn W Polsce będą jednak stosowane szybkie testy na koronwirusa,…

Ten post dostępny jest także w języku: English Facebook Twitter LinkedIn Grudziądzki Holding Komunalny ma pomóc w poprawie sytuacji finansowej…

Ta strona korzysta z ciasteczek, aby zapewnić Ci najlepszą możliwą obsługę. Informacje o ciasteczkach są przechowywane w przeglądarce i wykonują funkcje takie jak rozpoznawanie Cię po powrocie na naszą stronę internetową i pomaganie naszemu zespołowi w zrozumieniu, które sekcje witryny są dla Ciebie najbardziej interesujące i przydatne.
Niezbędne ciasteczka powinny być zawsze włączone, abyśmy mogli zapisać twoje preferencje dotyczące ustawień ciasteczek.
Jeśli wyłączysz to ciasteczko, nie będziemy mogli zapisać twoich preferencji. Oznacza to, że za każdym razem, gdy odwiedzasz tę stronę, musisz ponownie włączyć lub wyłączyć ciasteczka.